2025
来源
温度新闻客户端
分享

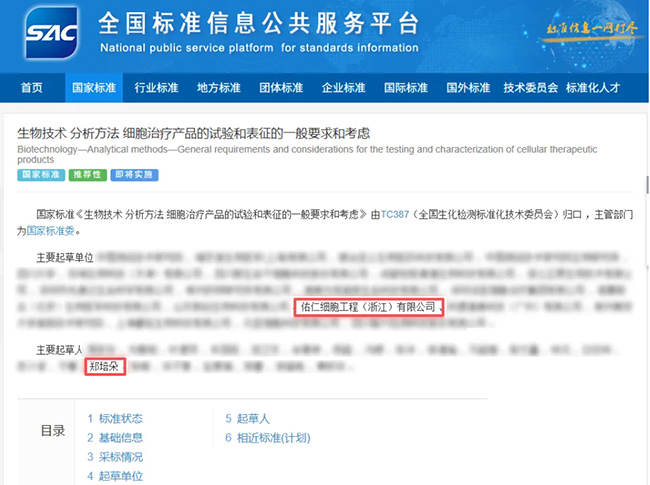
日前,国家市场监督管理总局(国家标准化管理委员会)发布公告,国家标准《生物技术分析方法细胞治疗产品的试验和表征的一般要求和考虑》(GB/T 46490-2025)正式批准发布,将于2026年5月1日起实施。该标准填补了国内细胞治疗产品试验与表征领域的标准空白,为行业规范化发展提供统一技术依据。该标准由位于瓯海区的佑仁细胞(浙江)有限公司为主要起草单位,公司董事长郑培朵博士担任主要起草人。

此次发布的国家标准内容涵盖细胞来源验证、生产工艺控制、质量评价体系等全链条关键环节,适用于免疫细胞、干细胞等各类细胞治疗产品。标准在制定过程中整合国际前沿技术要求,结合国内产业实际细化操作规范,明确国际标准分类号07.080(生物技术与生物医学),标志着我国细胞治疗领域标准化建设取得突破性进展。
业内人士指出,该标准的实施将从监管、研发、临床应用到产业竞争全链条产生深远影响:监管部门可依据统一标准提升审批效率;企业研发获得明确技术指南,降低试错成本;患者将受益于更稳定可靠的治疗产品;产业层面则通过标准推动优质资源整合,增强我国在全球细胞治疗领域的话语权。

佑仁细胞作为温州瓯海本土培育的细胞治疗领军企业,自成立以来持续投入细胞治疗技术研发,组建包含诺奖获得者、院士在内的顶尖科研团队,已参与多项行业标准制定工作。郑培朵表示,未来将继续深耕干细胞治疗领域,协同产业链伙伴共同推进标准化建设,助力行业高质量发展。
编辑: 夏卢克
本文转自:瓯海新闻网 ohnews.cn